Поскольку мы ввели шкалу температур, мы можем следующим образом определить количество теплоты. Назовем калорией количество теплоты, необходимое для нагрева 1 г воды от 14° до 15° по Цельсию. Совершенно не существенно, откуда берется тепло — от удара, трения или огня. Когда вода получает 1 кал, ее температура подымается на 1 градус. Или, когда у воды отбирается 1 кал, температура 1 г воды уменьшается на 1 градус по шкале Цельсия. Таким образом, стандартное количество теплоты определяется с помощью единицы изменения температуры и массы стандартного вещества (воды)1).
При таком определении количества теплоты создается впечатление, что мы считаем ее некоей субстанцией. Мы близки к тому, чтобы сказать такую фразу: при наливании 1 калории в 1 грамм воды температура воды увеличивается на 1 градус. Используемая нами терминология сохранилась с тех времен, когда теплоту считали жидкой субстанцией (теплородом). Хотя предмет может казаться очень холодным, это не значит, что он не содержит тепла. Например, кусок льда способен нагреть кусок сухого льда, причем сам он будет при этом охлаждаться. Куском же сухого льда можно повысить температуру жидкого гелия. (Есть ли у подобной последовательности предел?)
Одна калория тепла не обязательно изменит температуру 1 грамма какого-либо вещества, отличного от воды, на 1 градус. Например, 1 г меди нагревается на 10,9°, если его снабдить 1 кал тепла. Эта относительная способность различных веществ поглощать различные количества тепла при увеличении их температуры на одну и ту же величину называется удельной теплоемкостью вещества (одно вещество поглощает больше тепла, чем другое, причем их температуры изменяются на одну и ту же величину). Она определяется как количество калорий, необходимое для увеличения температуры 1 г вещества на 1 градус по шкале Цельсия. Например, удельная теплоемкость меди равна 0,092 кал/г*град С.
1) Следует иметь в виду, что, если мы хотим предложить наиболее разумное определение, мы должны соблюдать особую осторожность в отношении тех факторов, значение которых мы не в состоянии полностью оценить в данный момент. (Какова, например, роль давления, испытываемого граммом воды? Одинаковое ли количество калорий требуется для нагрева того же грамма воды с 18 до 19°С или с 78 до 79°С?)
Многие вещества обладают тем свойством, что их удельные теплоемкости остаются практически постоянными при изменении температуры в широких пределах. Так, 1 кал тепла увеличивает температуру 1 г воды приблизительно на 1° независимо от ее начальной температуры. 
Однако в точках замерзания или кипения, как правило, вещества поглощают сравнительно большое количество теплоты, а температура их при этом не изменяется. Например, чтобы расплавить лед при 0° С, требуется 80 кал на 1 г льда. Чтобы выпарить 1 г кипящей воды, необходимо 540 кал. Поэтому плавающие2) в воде кубики льда поддерживают в ней температуру 0° С, ибо любое тепло, которое поступает в систему вода — лед, идет на таяние льда, а отток тепла вызывает замерзание воды, но в обоих случаях не происходит изменения температуры (фиг. 358).
2) Почти все вещества при охлаждении сокращаются в объеме и становятся более плотными. Исключение составляет вода, которая аномально расширяется при замерзании, поэтому лед при 0°С менее плотен, чем вода при той же температуре. В результате лед плавает на поверхности озер и океанов, способствуя сохранению тепла, в толще воды. Благодаря этому вода остается жидкой, а лед не опускается на дно, что привело бы к утечке тепла, и замораживанию всей толщи воды. Такое поведение воды при замерзании имеет существенное значение для рыб, нашего климата и всей нашей жизни.
Теплота является сохраняющейся величиной (не создается и не уничтожается) только в изолированных системах, т. е. системах, откуда тепло не выходит и куда оно не входит. Если опустить нагретую ложку в изолированный сосуд с холодной водой, то ложка будет охлаждаться, а вода нагреваться до тех пор, пока их температуры не сравняются. 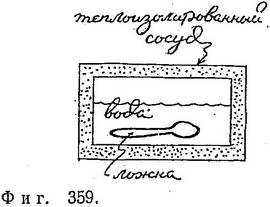
При данных массах ложки и воды и заданных начальных температурах конечная температура всегда, будет одной и той же, как. будто полное тепло так распределяется между всеми частями системы, что уравнивает их температуры (т. е. наступает тепловое равновесие).
Для системы, показанной на фиг. 359:
Если ложка медная (удельная теплоемкость 0,092 кал/г*град С), ее масса равна 10 г, начальная температура 100° С, а масса воды равна 100 г и ее начальная температура 20° С, то тепло, потерянное ложкой = 10*0,092*(100—Т), а тепло, полученное водой = 100*1*(Т—20), где Т — окончательная температура системы. Следовательно,
0,92 (100—Т) = 100 (Т—20); 100,92Т = 2092, Т ≈ 20,8°С, (24.3)
Тот факт, что тела нагреваются при соударениях или трении друг о друга, послужил, вероятно, причиной тому, что теплоту издавна считали как-то связанной с движением. В 1620 г. Фрэнсис Бэкон заявил, что «Теплота сама по себе… есть движение и ничего более». Он пришел к такому заключению, наблюдая, как возникает тепло при столкновениях твердых тел или трении их друг о друга. Позднее Роберт Бойль и Роберт Гук высказывали такую же идею. Однако в те времена она не имела большого успеха, так как никто не мог объяснить, почему, если теплота есть движение, оно сохраняется в экспериментах, подобных описанному выше, в которых смешивались различные вещества при различных температурах в термически изолированных сосудах.
В восемнадцатом веке появилась теория, согласно которой теплота считалась тонким упругим флюидом, частицы которого отталкиваются друг от друга, но притягиваются частицами обычных веществ. Этот флюид получил название caloric — теплород («caloric» — слово, придуманное позднее, в 1787 г., Лавуазье), а теория, описывающая теплоту в виде материальной субстанции, — название материальной, или субстанциональной, теории теплоты.
В основе материальной теории лежала мысль о том, что теплота сохраняется. Большинство наблюдений и экспериментов тех времен проводилось при весьма специфических условиях, при которых полное количество теплоты (в том смысле, как тогда было принято) сохранялось, из чего и делался вывод, что теплота — сохраняющаяся величина. Было очень удобно считать, что теплота есть субстанция, которая не исчезает и не возникает из ничего, но перетекает от одного тела к другому. Частицы вещества, если считать, что они не могут проникать друг сквозь друга, не могут находиться между собой в контакте, несмотря на взаимное притяжение. (Иначе вещества нельзя было бы сжимать.) Поэтому между частицами должна действовать какая-то уравновешивающая притяжение сила, и эта сила была приписана действию теплорода. Из-за того, что частицы теплорода взаимно отталкиваются, теплота должна перетекать от нагретого тела к холодному. Согласно этой теории, состояние вещества — твердое, жидкое или газообразное — определяется количеством теплорода, входящего в его состав. Когда вещество содержит много теплорода, оно становится газообразным. Из-за взаимного расталкивания частиц теплорода наличие большого его количества в веществе приводит к тому, что силы расталкивания превосходят силы притяжения между частицами вещества и вынуждают последние оставаться свободными. Считалось, что при охлаждении тел теплород покидает их, что согласовывалось с сокращением большинства тел при охлаждении. Твердые и жидкие тела содержат меньше теплорода, чем газообразные, и поэтому занимают меньшие объемы.
Хотя материальная теория давно уже оставлена, некоторые ее термины сохранились в современной науке о теплоте, особенно в тех разделах, где рассматриваются потоки и перенос тепла. Мы по-прежнему говорим, что тепло течет, а тело поглощает тепло. Это приводит к некоторой путанице, поскольку мы говорим о теплоте как о какой-то субстанции, даже если мы знаем, что на самом деле это не так.
Бенджамин Томпсон, граф Румфорд (1753—1814), американский эмигрант, которому посчастливилось провести свои последние годы в Париже, автор почти картезианского изречения: «Ясно, что в философских исследованиях нет ничего более опасного, чем принимать что-либо на веру, как бы правдоподобно оно ни выглядело, пока оно не будет доказано прямым и решающим экспериментом» и человек легендарной энергии, выбрал в качестве одного из своих занятий «науку о Теплоте, науку, несомненно, первостепенной важности для человечества!». Его интерес к «этому удивительному предмету» возник, по его словам, следующим образом:
«Обедая, я часто замечал, что некоторые блюда сохраняют свое тепло гораздо дольше других, а яблочные пироги и яблоки с миндалем (одно из любимых английских кушаний) оставались горячими удивительно долго. Сильно пораженный такой необычной способностью сохранять теплоту, которой обладали яблоки, я часто размышлял о ней; и, обжигая яблоками рот или встречая другие блюда с такими же свойствами, я всегда пытался, но все напрасно, найти хоть какое-нибудь удовлетворительное объяснение этому удивительному явлению».
То, что Румфорд обжигал свой рот рисовым супом, а позднее — руки в горячих банях Неаполя, не уменьшало его интерес к этой проблеме. Наоборот, он решился провести почти классическую серию экспериментов, направленную против материальной теории теплоты3).
Можно утверждать, что если теплород — вещество, то он должен обладать основным свойством любого вещества и иметь массу. В своих экспериментах Румфорд, к своему удовлетворению, показал, что «все попытки обнаружить влияние тепла на веса тел бесплодны». Однако его доказательство невесомости теплорода не могло смутить сторонников материальной теории. Они могли возразить, что теплород, как в более ранние времена небесная субстанция, не является обычным веществом, и поэтому он не обязан подчиняться гравитационным силам.
Совершенно случайно («чисто случайно мне пришлось заниматься экспериментами, о которых я собираюсь рассказать») Румфорд заинтересовался вопросом о получении тепла с помощью трения.
«Позднее, заведуя сверлением пушечных стволов в мастерских военного арсенала в Мюнхене, я был сильно поражен тем значительным количеством тепла, которое за короткое время получает, медный ствол при сверлении, и еще большим количеством тепла (гораздо большим, как я выяснил из эксперимента, чем тепло, требуемое для закипания воды), которое получают металлические стружки, отделяемые от ствола сверлом».
С помощью материальной теории теплоты было трудно объяснить, откуда берется такое, большое количество теплорода. При желании, конечно, можно было ввести гипотезу, что силы притяжения между молекулами металла и частицами теплорода уменьшаются, когда металл превращается в стружку, в результате чего теплород освобождается и проявляется в виде теплоты.
Однако при сверлении запас тепла казался неистощимым. Этого было достаточно, чтобы убедить Румфорда:
«…мне кажется чрезвычайно трудно, если не совершенно невозможно, выдвинуть хоть какую-нибудь разумную идею, объясняющую то, что возбуждалось и передавалось в этих экспериментах, чем-либо отличным от движения».
3) Говорят, историки относятся к его работе гораздо серьезней, чем к ней отнеслись его современники.